肿瘤免疫治疗依赖于机体对肿瘤的精准识别与高效应答。其中,来源于肿瘤体细胞突变的新抗原因其高特异性和低免疫风险,被认为是极具潜力的个性化肿瘤疫苗候选分子。然而,新抗原多为疏水性和非极性氨基酸组成的短肽,普遍存在溶解性差、易聚集、免疫原性不足以及交叉递呈效率低等问题,严重制约了实际应用。如何在提升递送效率的同时增强免疫激活能力,是新抗原肿瘤疫苗的关键挑战。
天然糖萼作为细胞表面的关键多糖结构,在细胞识别与免疫应答中具有重要作用。受此启发,研究人员利用多糖或糖基材料作为免疫调节生物材料,可实现免疫应答的增强。然而,目前广泛使用的天然多糖多为商业化提取产物,其化学结构不明确、分子量分布极宽且常伴随杂质,使得材料结构与免疫功能之间的因果关系难以厘清,也限制了对分子机制的深入理解。在课题组前期提出的仿糖萼纳米结构的基础上(Small2015, 11, 4191; Biomacromolecules2018, 19, 2098; J. Am. Chem. Soc. 2025, 147, 38838),针对上述问题,我们进一步提出了一种基于糖聚合物的仿糖萼纳米疫苗策略,用于递送与增强新抗原的免疫原性。研究选用甘露聚糖天然结构片段的甘露糖与甘露二糖作为模型配体,它们均是C型凝集素受体(如DC-SIGN、Dectin-2)的经典识别单元。通过可控聚合方法,将甘露单糖苷或甘露二糖苷以侧链接枝方式精确引入酸敏性聚合物中,构建了具有明确化学结构的糖聚合物。其在水溶液中自组装形成稳定纳米颗粒,并在表面呈现高密度糖基结构,可以模拟天然糖萼与免疫细胞的相互作用。
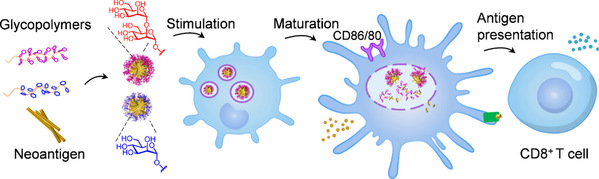
图1.用于递送和增强肿瘤新抗原免疫原性的仿糖萼纳米疫苗
进一步通过与新抗原进行共组装,发现该仿糖萼纳米载体不仅显著改善了新抗原的溶解性与分散性,还可通过与树突状细胞(DC细胞)表面的C型凝集素受体结合,促进高效内吞并诱导DC细胞成熟。同时,聚合物中引入的酸敏单元使纳米颗粒在内涵体弱酸环境中发生解体并产生“质子海绵效应”,有效促进新抗原逃逸至胞质,从而增MHC I途径介导的抗原交叉递呈。相比甘露单糖苷修饰的聚合物,甘露二糖苷修饰的纳米疫苗表现出更强的受体结合能力和免疫激活效果,在通过DC细胞呈递之后,可显著促进CD8⁺细胞毒性T细胞的增殖及 IFN-γ、IL-2等促炎性细胞因子的分泌。总的来说,该工作提出了一种集递送功能与内源性免疫佐剂效应于一体的仿糖萼纳米疫苗策略,表明了人工糖萼结构不仅可作为生物相容性的纳米载体,还可通过精确的糖基排列与刺激响应行为直接参与免疫调控,为肿瘤新抗原疫苗及亚单位疫苗的理性设计提供了新的思路。
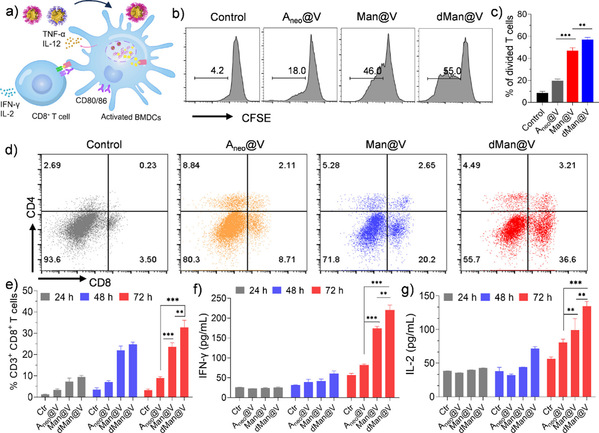
图2.仿糖萼纳米疫苗增强新抗原的交叉呈递及CD8+T细胞的增殖和活化
上述研究结果近日发表于ACS Macro Lett.2026, 15, 165–173上,文章链接https://pubs.acs.org/doi/10.1021/acsmacrolett.5c00712。论文第一作者为博士生史怡炜,通讯作者为李龙助理教授。课题组陈国颂教授和已毕业博士生徐旭阳为本工作的完成提供了重要支持。
